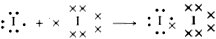En este link:
http://www.udbquim.frba.utn.edu.ar/quiz/index.html?file=sol.js
encontraras un examne corto acerca de soluciones
Rafael Borneo. PhD. Profesor Asociado. Cátedra Química. Universidad Nacional de Córdoba. Argentina
29/8/11
28/8/11
Como se prepara una solucion?
Mira este video para que tengas una idea de como se prepara una solucion en el laboratorio a partir de drogas solidas
Soluciones Practica Online
En este SITIO puedes practicar conceptos basicos de Soluciones online. Son 21 preguntas. Hay algunas que no podras hacer ya que no la vemos en clase. A TRABAJAR que YA VIENE EL EXAMEN
Unidades Quimicas de Concentracion

Para expresar la concentración de una solución se pueden usar unidades químicas aunque la idea general es siempre expresar la cantidad de soluto en una cantidad de solución.
Fracción molar: Usando el concepto de mol se puede expresar la concentración de una solución como la cantidad de un componente i cualquiera (en moles) en la cantidad total de todos los componentes de la solución (en moles):
Xi (fracción molar de i) = moles de i / (moles de i + moles de j + moles de k + ....)
y que la suma de Xi + Xj + Xk..... = 1
Molaridad
La molaridad (M) se define como la cantidad de moles de soluto en un litro de solución M = moles de soluto / volumen de solución (L)
Molalidad
La Molalidad se define como los moles de soluto presentes en un Kilogramo de disolvente (NO SOLUCION)
Unidades Fisicas de Concentracion
La concentración de una solución es la medida de la cantidad de soluto presente en una cantidad de solución (o disolvente). Existen varias maneras de describir la concentración de una solución.
Unidades Físicas. Porcentajes
Por definición el porcentaje es la proporción (en partes) por cada 100 partes de un todo. Si aplicamos este concepto a las disoluciones podemos definir la concentración de una solución como partes de soluto en 100 partes de solución. Las “partes” puedes ser expresadas en Masa (g) o volúmenes (mL, L).
Si se disuelven 2 g de NaCl en 98 g de Agua se obtienen 100 g de una solución que es
2 por ciento (%) de masa (sal). Específicamente esta solución se describiría como 2 % (peso/peso) de sal en agua [lo cual quiere decir que son 2 g (peso) en 100 g (peso) de solución)]
Si ahora disolvemos 5 L metanol (volumen) en 95 L de agua tendremos una solución 5% (volumen/volumen ó vol./vol.)
Otra posibilidad es expresar el peso de soluto en 100 volúmenes de solución. Así una solución de 0,5 g (peso) en 100 mL (volumen) de solución sería una solución 0,5% (peso/volumen ó P/V)
Como se calcula el rendimiento de una reaccion?
Rendimiento de una reacción
La cantidad de producto que se obtiene si reacciona todo el reactivo limitante se denomina el rendimiento teórico de la reacción.
La cantidad de producto que se obtiene realmente en una reacción es el rendimiento real
Rendimiento real es generalmente menor que el teórico
Razones para explicar la diferencia entre el rendimiento real y el teórico:
-Muchas reacciones son reversibles, de manera que no proceden 100% de izquierda a derecha.
- Aún cuando una reacción se complete en un 100%, resulta difícil recuperar todo el producto del medio de la reacción
- Los productos formados pueden seguir reaccionando entre sí o con los reactivos, para formar todavía otros productos. Estas reacciones adicionales reducen el rendimiento de la primera reacción.
El rendimiento porcentual o porcentaje del rendimiento describe la relación del rendimiento real y el rendimiento teórico:
Por ejemplo si teóricamente se formaran 1100 g de un compuesto en una reacción química pero en realidad se forman solo 900 g el porcentaje de rendimiento sería:
(900 g/1100g) x 100 = 84.81%
La cantidad de producto que se obtiene si reacciona todo el reactivo limitante se denomina el rendimiento teórico de la reacción.
La cantidad de producto que se obtiene realmente en una reacción es el rendimiento real
Rendimiento real es generalmente menor que el teórico
Razones para explicar la diferencia entre el rendimiento real y el teórico:
-Muchas reacciones son reversibles, de manera que no proceden 100% de izquierda a derecha.
- Aún cuando una reacción se complete en un 100%, resulta difícil recuperar todo el producto del medio de la reacción
- Los productos formados pueden seguir reaccionando entre sí o con los reactivos, para formar todavía otros productos. Estas reacciones adicionales reducen el rendimiento de la primera reacción.
El rendimiento porcentual o porcentaje del rendimiento describe la relación del rendimiento real y el rendimiento teórico:
Por ejemplo si teóricamente se formaran 1100 g de un compuesto en una reacción química pero en realidad se forman solo 900 g el porcentaje de rendimiento sería:
(900 g/1100g) x 100 = 84.81%
Que es Reactivo limitante?
Supongamos que tenemos que preparar 10 pebetes de jamón y queso. Para preparar un pebete se necesitan un pan, una feta de jamón y otra de queso. Hay 10 panes, 10 fetas de queso y 8 de jamón. Podremos preparar solamente 8 pebetes de jamón y queso y ni uno más porque no hay más jamón. Decimos entonces que el jamón es el ingrediente limitante del número de pebetes a preparar.
En una reacción química la situación es similar: una vez se haya consumido uno de los reactivos la reacción se detiene.
CH4(g) + 2O2(g) = CO2(g) + 2H2O (l)
CH4(g) + 2O2(g) = CO2(g) + 2H2O (l)
Así ,si queremos obtener 2 moles de agua necesitaremos partir de 1 mol de metano y dos moles de oxígeno (porque la estequiometría de la reacción es 1 moles de metano reaccionan con 2 moles de oxígeno para dar dos moles de agua).
Que pasaría si en lugar de dos moles de oxigeno tenemos solo 1 mol??
Una vez haya reaccionado todo el oxigeno nos quedara sobrando metano sin reaccionar y se habrán obtenido solo un mol de agua, es decir, entonces la reacción se terminara cuando medio (1/2) mol de metano haya reaccionado un mol de oxigeno (todo el oxigeno presente).
Al reactivo que se ha consumido en su totalidad en una reacción química se le denomina reactivo limitante, ya que limita la cantidad de producto formado. Así en el ejemplo anterior el oxigeno era el reactivo limitante, ya que con los 1 mol de oxígeno solo medio mol de metano reacciona (y sobra medio mol de metano)
¿Cómo hacer para saber cuál es el reactivo limitante de una reacción?
Calculando los moles de producto que se obtienen con cada reactivo, suponiendo que el resto de reactivos están en cantidad suficiente. Aquel reactivo que nos dé el menor número potencial de moles de producto es el reactivo limitante. Al resto de reactivos, presentes en mayor cantidad que la necesaria para reaccionar con la cantidad del reactivo limitante, se les denomina reactivos en exceso.
Ejemplo:
Considere la siguiente reacción:
CH4(g) + 2O2(g) = CO2(g) + 2H2O (l)
Suponga que se mezclan 2 g de CH4 con 10 g de O2. Quien es el reactivo limitante?? Cuanto se puede obtener de agua y dióxido de carbono?
1. Primero tenemos que convertir los gramos de reactivos en moles:
1 mol de CH4 pesa 16 gramos (12 del C + 4 del H) por lo que 2 gramos serán (por regla de tres) 0,125 moles
1 mol de O2 pesa 32 gramos por lo que 10 gramos serán (por regla de tres) 0,3125 moles
2. Luego definimos la proporción estequiométrica entre reactivos y productos:
1 mol de metano reacciona con dos moles de oxigeno
3. Calculamos el número de moles de reactivos que se consumirían si cada reactivo se consumiese en su totalidad:
0,125 moles de metano reaccionarían con 0,125x2 moles de oxigeno = 0,25 moles de oxigeno
0,3125 moles de oxigeno reaccionaría con 0,3125/2 moles de metano = 0,15625 moles de metano
Entonces:
4. El reactivo limitante es el metano y podremos obtener como máximo 0.125 moles de dióxido de carbono (relación 1 mol de metano 1 mol de dióxido) y 0.25 moles de agua (relación 1mol de metano dos de agua). Además, sobraran 0,0625 moles de oxigeno (0,3125 moles iniciales menos 0,25 moles que reaccionaron).
20/8/11
Enlace Metalico
La plata, un metal típico, consiste en una formación regular de átomos de plata que han perdido cada uno un electrón para formar un ion plata. Los electrones negativos se distribuyen por todo el metal formando enlaces no direccionales o deslocalizados con los iones plata positivos. Este modelo, conocido como enlace metálico, explica las propiedades características de los metales: son buenos conductores de la electricidad al estar los electrones libres para moverse de un sitio a otro, y resultan maleables porque sus iones positivos se mantienen unidos por fuerzas no direccionales
Enlace Ionico
El Cloruro de Sodio (NaCl) esta formado por un atomo de sodio y uno de cloro. Ambos se mantienen unido por una furza electrostatica generada por la formacion de iones producto de una transferencia de electrones.
Debido a la transferencia de electrones el sodio se transforma en catión (ion de carga positiva) y el cloro en anión (ion de carga negativa). Este intercambio de electrones se refleja en la diferencia de tamaño entre los átomos antes y después del enlace (izquierda).
Atraídos por fuerzas electrostáticas los iones se organizan formando una red cristalina en la que cada uno es fuertemente atraído hacia un grupo de ‘vecinos próximos’ de carga opuesta y, en menor medida, hacia todos los demás iones de carga opuesta a través de todo el cristal.
Debido a la transferencia de electrones el sodio se transforma en catión (ion de carga positiva) y el cloro en anión (ion de carga negativa). Este intercambio de electrones se refleja en la diferencia de tamaño entre los átomos antes y después del enlace (izquierda).
Atraídos por fuerzas electrostáticas los iones se organizan formando una red cristalina en la que cada uno es fuertemente atraído hacia un grupo de ‘vecinos próximos’ de carga opuesta y, en menor medida, hacia todos los demás iones de carga opuesta a través de todo el cristal.
Enlace Covalente. Polaridad
Una manera de clasificar los enlaces covalentes es según su polaridad.
a) Enlace covalente apolar o no polar
a) Enlace covalente apolar o no polar
Entre átomos idénticos o diferentes pero de igual electronegatividad DEN=0, los electrones se comparten de igual forma por ambos. A este tipo de enlace se lo denomina enlace covalente apolar.
Podemos citar los ejemplos del Hidrógeno (visto en enlace covalente simple), oxígeno (enlace covalente doble), Nitrógeno (enlace covalente triple) o PH3 ( 3 enlaces simples).
b) Enlace covalente polar
En cambio, si los dos átomos enlazados difieren como en el caso del H:Cl, o son idénticos, pero sus vecinos no lo son, como en el caso de los dos átomos de C en H3C--CCl3 , los electrones no se comparten por igual: uno de los átomos (el más electronegativo) atrae electrones con más fuerza que el otro. El átomo que ejerce la mayor atracción desarrolla una cierta carga negativa; el otro adquiere una cierta carga positiva. Estas cargas son inferiores a la unidad, -1 o +1 y se llaman cargas parciales, representadas como d+ y d-.
Así, dado que el cloro es más electronegativo que el hidrógeno, el cloruro de hidrógeno se representa:
d- d+
..
:Cl -H :
..
Estos enlaces covalentes son polares, para diferenciarlos de los enlaces Cl--Cl o H--H que son no polares. El caso límite de desigualdad en los electrones compartidos es el enlace iónico en los compuestos CsF, NaCl o CaF2. Por lo tanto, el enlace covalente no polar y el enlace iónico son casos extremos de la distribución de un par de electrones entre dos núcleos. Entre estos dos extremos se encuentran situados los enlaces covalentes polares.
Las moléculas diatómicas con enlace covalente polar presentan, obviamente, momento dipolar no nulo. En el caso de las moléculas triatómicas, la presencia de enlaces polares no garantiza que la molécula sea polar. Lo mismo ocurrirá en moléculas con mayor número de átomos.
El CO2 presenta enlaces C-O que son polares ya que los átomos tienen distinta electronegatividad; como la molécula es lineal (el ángulo OCO es 180°) , los vectores momento dipolar generados por cada enlace resultan opuestos y ,debido a que son de igual magnitud, el momento dipolar resultante es cero. En cambio, la molécula de H2O es angular (el ángulo HOH es distinto de 180° ), de modo que la composición de los dos vectores momento dipolar resulta en un momento dipolar no nulo (en rigor, bastante elevado).
Enlace Quimico. Tipos
Los enlaces químicos resultan de interacciones electrostáticas y se los clasifican en tres grandes grupos, enlace iónico, enlace covalente y enlace metálico.
1) Enlace iónico: resulta de las interacciones electrostáticas entre iones de cargas opuestas.
2) Enlace covalente: es el resultado de compartir electrones entre dos átomos.
3) Enlace metálico: cada átomo está unido a varios átomos vecinos por electrones que son relativamente libres de moverse a través de la estructura tridimensional.
1) Enlace iónico: resulta de las interacciones electrostáticas entre iones de cargas opuestas.
2) Enlace covalente: es el resultado de compartir electrones entre dos átomos.
3) Enlace metálico: cada átomo está unido a varios átomos vecinos por electrones que son relativamente libres de moverse a través de la estructura tridimensional.
Material de vidrio
Como ya Uds. saben una de las cosas que mas se usan en un laboratorio de química es el material de vidrio. Si quieren pueden ver el material de vidrio de uso comun en el laboratorio tales como pipetas, matraces, vasos de precipitado, etc. Asi que vayan a este sitio y fijense en el material de vidrio que alli se presenta. Espere que esto les ayude a clarificar lo visto en el laboratorio.
 |
| Vaso de precipitado |
 |
| Matraz |
 |
| Pipeta Volumetrica |
 |
| Bureta |
14/8/11
Enlace Quimico. Introduccion.
Ante la diversidad de elementos químicos existentes en la naturaleza cabe preguntarse cuál es la razón por la que unos átomos se reúnen formando una molécula y otros no; o de otra manera, por qué no toda molécula o agrupación de átomos imaginable tiene existencia real. Una primera respuesta puede hallarse en la tendencia observada en todo sistema físico a alcanzar una condición de mínima energía. Aquella agrupación de átomos que consiga reducir la energía del conjunto dará lugar a una molécula, definiendo una forma de enlace químico que recibe el nombre de enlace covalente.
Junto con esa idea general de configuración de energía mínima, otros intentos de explicación de este tipo de enlace entre átomos han sido planteados recurriendo a las características fisicoquímicas de las estructuras electrónicas de los átomos componentes.
La teoría de Lewis
El químico estadounidense G. B. Lewis (1875-1946) advirtió que el enlace químico entre átomos no podía explicarse como debido a un intercambio de electrones. Dos átomos iguales intercambiando electrones no alterarían sus configuraciones electrónicas; las ideas válidas para el enlace iónico no eran útiles para explicar de una forma general el enlace entre átomos. Sugirió entonces que este tipo de enlace químico se formaba por la comparación de uno o más pares de electrones o pares de enlace. Por este procedimiento los átomos enlazados alcanzaban la configuración electrónica de los gases nobles. Este tipo de configuración de capas completas se corresponde con las condiciones de mínima energía o máxima estabilidad características de la situación de enlace.
La teoría de Lewis, conocida también como teoría del octete por ser éste el número de electrones externos característicos de los gases nobles, puede explicar, por ejemplo, la formación de la molécula de yodo I2:
La teoría de Lewis, conocida también como teoría del octete por ser éste el número de electrones externos característicos de los gases nobles, puede explicar, por ejemplo, la formación de la molécula de yodo I2:
Ambos átomos, que individualmente considerados tienen siete electrones en su capa externa, al formar la molécula de yodo pasan a tener ocho mediante la comparación del par de enalce .
Existen moléculas cuya formación exige la comparación de más de un par de electrones. En tal caso se forma un enlace covalente múltiple. Tal es el caso de la molécula de oxígeno O2:
Existen moléculas cuya formación exige la comparación de más de un par de electrones. En tal caso se forma un enlace covalente múltiple. Tal es el caso de la molécula de oxígeno O2:
para cuya formación se comparten dos pares de electrones. Representado cada par de electrones mediante una línea resulta:
que indica más claramente la formación de un doble enlace.
En la molécula de nitrógeno N2 sucede algo semejante, sólo que en este caso se han de compartir tres pares de electrones para alcanzar el octete, con la formación consiguiente de un triple enlace:
En la molécula de nitrógeno N2 sucede algo semejante, sólo que en este caso se han de compartir tres pares de electrones para alcanzar el octete, con la formación consiguiente de un triple enlace:
 Esta explicación puede extenderse al caso de las moléculas formadas por átomos de elementos no metálicos diferentes entre sí, tales como HCl o NH3 por ejemplo:
Esta explicación puede extenderse al caso de las moléculas formadas por átomos de elementos no metálicos diferentes entre sí, tales como HCl o NH3 por ejemplo:
Lewis contempló la posibilidad extrema de que los pares electrónicos de enlace fueran aportados por un sólo átomo. Tal es el caso del ion amonio en el cual el atomo de nitrogeno aporta el par de electrones al enlace con el ion H+:
Los subíndices que aparecen en las fórmulas químicas de compuestos covalentes expresan el número de átomos que se combina para formar una molécula y están, por tanto, relacionados con la capacidad de enlace de cada uno de ellos, también llamada valencia química. Según la teoría de Lewis, la configuración electrónica de la capa externa condiciona dicha capacidad y es la responsable del tipo de combinaciones químicas que un determinado elemento puede presentar.
La teoría del enlace de valenciaLa superación del modelo de Bohr y el desarrollo del modelo atómico de la mecánica cuántica tuvo una clara repercusión en las ideas sobre el enlace químico en general y sobre el covalente en particular. Uno de los enfoques mecanocuánticos del enlace covalente se conoce como teoría del enlace de valencia y permite comprender en términos no sólo de energías, sino también de fuerzas, el fenómeno del enlace entre átomos.
La formación del enlace covalente simple tiene lugar cuando los orbitales correspondientes a dos electrones desapareados de átomos diferentes se superponen o solapan, dando lugar a una región común en la cual los dos electrones con espines opuestos, tal y como exige el principio de exclusión de Pauli, ocupan un mismo orbital. Ese par compartido constituye el elemento de enlace entre los dos átomos. Así, por ejemplo, cuando dos átomos de H se aproximan suficientemente, existe una disposición en la cual sus nubes electrónicas están parcialmente solapadas y para la que la energía potencial del conjunto es mínima, constituyendo, pues, una situación de enlace. En términos electrónicos puede afirmarse que el orbital 1s de cada átomo de hidrógeno, semiocupado por su electrón correspondiente, es completado por el electrón del otro átomo de hidrógeno. Los dos electrones con espines opuestos de este par, son atraídos entonces por cada uno de los núcleos, constituyendo el par de enlace. La existencia de este par común es lo que determina que los núcleos estén ligados entre sí con las limitaciones que, en cuanto a proximidad, imponen las fuerzas de repulsión nuclear.
La idea de comparación de electrones de Lewis sigue, de algún modo, presente en la teoría del enlace de valencia, aunque se abandona la regla del octete y se sustituye por la condición de que dos electrones desapareados puedan ocupar un mismo orbital. El número de enlaces covalentes posible depende, entonces, del número de electrones desapareados presentes en el átomo correspondiente o en algún estado excitado previo a la formación de la molécula
chemistry education, chemical bonds, practices of laboratory, lab work, problems and solutions
Gases Inertes o Nobles
Los gases nobles son incoloros, inodoros, insípidos y no inflamables en condiciones normales. Los gases nobles (tambien conocidos como gases inertes) presentan una reactividad química muy baja. Los seis gases nobles que se encuentran en la naturaleza son helio (He), neón (Ne), argón (Ar), kriptón (Kr), xenón (Xe) y el radioactivo radón (Rn). Se sitúan en el grupo 18 (8A) de la tabla periódica (anteriormente llamado grupo 0). Antiguamente, se creía que tenían una valencia cero y que sus átomos no se puedían combinar con otros elementos (gases inertes). El último nivel de electrones (capa de valencia) de los gases nobles esta lleno de electrones extremadamente estables y por tanto no tienden a formar enlaces químicos. Por tanto, tienen poca tendencia a ganar o perder electrones y de allí su baja reactividad.
A continuación la configuración electrónica de los principales gases nobles:
Helio (Z =2): 2
Neón 2 (Z =10): 8
argón (Z =18): 2: 8, 8
kriptón (Z =36): 2, 8, 18, 8
xenón (Z =54): 2, 8, 18, 18, 8
radón (Z =86): 2, 8, 18, 32, 18, 8
A continuación la configuración electrónica de los principales gases nobles:
Helio (Z =2): 2
Neón 2 (Z =10): 8
argón (Z =18): 2: 8, 8
kriptón (Z =36): 2, 8, 18, 8
xenón (Z =54): 2, 8, 18, 18, 8
radón (Z =86): 2, 8, 18, 32, 18, 8
Los Halogenos: CLoro, Cromo, Fluor, etc
Los halógenos son los elementos químicos de la tabla periódica que conforman el grupo 17 (anteriormente grupo VII A): flúor, cloro, bromo, yodo y astato. Los halógenos se encuentran en la naturaleza formando moléculas bi-atómicas químicamente activas X2. La actividad química se debe a que en su último nivel energético tienen una configuración electrónica s2p5, faltándole un electrón para completar el máximo de 8. Los halógenos tienen tendencia a formar un ión mononegativo, X-. Este anión se denomina haluro; las sales que lo contienen se conocen como haluros.
Los miembros de este grupo de la tabla periódica poseen una electronegatividad ≥ 2,5 según la escala de Pauling, presentando el flúor la mayor electronegatividad, y disminuyendo ésta al bajar en el grupo. Son elementos oxidantes (disminuyendo esta característica al bajar en el grupo), y el flúor es capaz de llevar a la mayor parte de los elementos al mayor estado de oxidación que presentan.
Los miembros de este grupo de la tabla periódica poseen una electronegatividad ≥ 2,5 según la escala de Pauling, presentando el flúor la mayor electronegatividad, y disminuyendo ésta al bajar en el grupo. Son elementos oxidantes (disminuyendo esta característica al bajar en el grupo), y el flúor es capaz de llevar a la mayor parte de los elementos al mayor estado de oxidación que presentan.
Metales alcalinos terreos
* Tienen configuración electrónica ns2.
* Tienen baja energía de ionización, aunque mayor que los alcalinos del mismo período
* A excepción del berilio, forman compuestos claramente iónicos.
* Son metales de baja densidad, coloreados y blandos.
* La solubilidad de sus compuestos es bastante menor que sus correspondientes alcalinos.
* Todos tienen sólo dos electrones en su nivel energético más externo (Todos tienen como valencia +2), con tendencia a perderlos, con lo que forman un ion positivo.
* Reaccionan con facilidad con halógenos para formar sales iónicas.
M + X2 — MX2
* Reaccionan con agua, aunque no tan rápidamente como los alcalinos, para formar hidróxidos fuertemente básicos.
M + 2 H2O — M(OH)2 + H2
* Tienen baja energía de ionización, aunque mayor que los alcalinos del mismo período
* A excepción del berilio, forman compuestos claramente iónicos.
* Son metales de baja densidad, coloreados y blandos.
* La solubilidad de sus compuestos es bastante menor que sus correspondientes alcalinos.
* Todos tienen sólo dos electrones en su nivel energético más externo (Todos tienen como valencia +2), con tendencia a perderlos, con lo que forman un ion positivo.
* Reaccionan con facilidad con halógenos para formar sales iónicas.
M + X2 — MX2
* Reaccionan con agua, aunque no tan rápidamente como los alcalinos, para formar hidróxidos fuertemente básicos.
M + 2 H2O — M(OH)2 + H2
Metales alcalinos
Los metales alcalinos son aquellos elementos químicos del grupo 1 (el que esta mas hacia la izquierda) de la tabla periódica (excepto el Hidrógeno que es un gas). Todos los metales alcalinos poseen un solo electrón en su nivel más externo. Tienen tendencia a perder este electrón y a reaccionar facilmente con los no metales (esto es debido a que tienen poca afinidad electrónica, y baja energía de ionización), Los metales alcalinos son los del grupo 1 y la configuración electrónica del grupo es ns¹. Por ello se dice que se encuentran en la zona "s" de la tabla.
Tabla Periodica
En este link:
encontraran la Tabla periodica de los Elementos. La tabla es interactiva por lo que pueden cliquear en un elemento o en un grupo o periodo y descubrir las propiedades de ese elemento, grupo o periodo. Indudablemente, una ayuda interesante para conocer la Tabla Periodica de los Elementos

encontraran la Tabla periodica de los Elementos. La tabla es interactiva por lo que pueden cliquear en un elemento o en un grupo o periodo y descubrir las propiedades de ese elemento, grupo o periodo. Indudablemente, una ayuda interesante para conocer la Tabla Periodica de los Elementos

Que son los isótopos?
 Los isótopos son átomos que tienen el mismo número atómico, pero diferente número másico, lo cual quire decir que un mismo elemento puede "pesar" diferente. La mayoría de los elementos tiene dos ó más isótopos. La diferencia en peso entre dos isótopos de un elemento es el número de neutrones en el núcleo. Fijese en la figura de la izquierda (cortesia de paxprofundis.org) en donde se muestran tres atomos, todos del Hidrogeno. Cual es la diferencia entre estos tres atomos?)
Los isótopos son átomos que tienen el mismo número atómico, pero diferente número másico, lo cual quire decir que un mismo elemento puede "pesar" diferente. La mayoría de los elementos tiene dos ó más isótopos. La diferencia en peso entre dos isótopos de un elemento es el número de neutrones en el núcleo. Fijese en la figura de la izquierda (cortesia de paxprofundis.org) en donde se muestran tres atomos, todos del Hidrogeno. Cual es la diferencia entre estos tres atomos?)El número de neutrones de un elemento químico se puede calcular como A-Z, es decir, como la diferencia entre el número másico y el número atómico. Por ejemplo, para el carbono Z=6. Es decir, todos los átomos de carbono tienen 6 protones y 6 electrones. Sin embargo, el carbono tiene dos isótopos: uno con A=12, con 6 neutrones y otro con número másico 13 (7 neutrones), que se representan como:
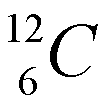
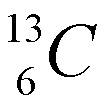
La cantidad relativa de un isótopo en la naturaleza recibe el nombre de abundancia isotópica natural. La masa atómica de un elemento es una media de las masas de sus isotópos naturales ponderada de acuerdo a su abundancia relativa. Por ejemplo, La plata (Ag) en su estado natural está constituida por una mezcla de dos isótopos de números másicos 107 y 109. Sabiendo que abundancia isotópica es la siguiente: 107Ag =56% y 109Ag =44%, el peso atómico de la plata natural se calcula como:

En general las propiedades químicas de un elemento están determinadas fundamentalmente por los protones y electrones de sus átomos y en condiciones normales los neutrones no participan en los cambios químicos. Por ello los isótopos de un elemento tendrán un comportamiento químico similar, formarán el mismo tipo de compuestos y reaccionarán de manera semejante.
Que es masa atomica?
La masa atómica relativa de un elemento, es la masa en gramos de 6.02 ·1023 (10 elevado a la 23) átomos (número de Avogadro, NA) de ese elemento. La masa relativa de los elementos de la tabla periódica desde el 1 hasta el 105 esta situada en la parte inferior de los símbolos de dichos elementos.
El átomo de carbono, con 6 protones y 6 neutrones, es el átomo de carbono 12 y es la masa de referencia para las masas atómicas. Una unidad de masa atómica (u.m.a), se define exactamente como 1/12 de la masa de un átomo de carbono que tiene una masa 12 u.m.a. una masa atómica relativa molar de carbono 12 tiene una masa de 12 g en esta escala. Un mol gramo (abreviado, mol) de un elemento se define como el numero en gramos de ese elemento igual al número que expresa su masa relativa molar. Así, por ejemplo, un mol gramo de aluminio tiene una masa de 26.98 g y contiene 6.023 ·1023 átomos.
El átomo de carbono, con 6 protones y 6 neutrones, es el átomo de carbono 12 y es la masa de referencia para las masas atómicas. Una unidad de masa atómica (u.m.a), se define exactamente como 1/12 de la masa de un átomo de carbono que tiene una masa 12 u.m.a. una masa atómica relativa molar de carbono 12 tiene una masa de 12 g en esta escala. Un mol gramo (abreviado, mol) de un elemento se define como el numero en gramos de ese elemento igual al número que expresa su masa relativa molar. Así, por ejemplo, un mol gramo de aluminio tiene una masa de 26.98 g y contiene 6.023 ·1023 átomos.
Que es el atomo?
 La palabra átomo proviene del idioma griego y significa “no divisible” o “indivisible” por lo que el átomo se consideraría la particular mas pequeña de la materia que no se puede dividir. Este concepto fue inventado por Demócrito en el 400 ac y en aquella época se creía que el átomo era efectivamente la particula más pequeña posible de la materia (lo cual no es cierto ya que hay partículas subatómicas)
La palabra átomo proviene del idioma griego y significa “no divisible” o “indivisible” por lo que el átomo se consideraría la particular mas pequeña de la materia que no se puede dividir. Este concepto fue inventado por Demócrito en el 400 ac y en aquella época se creía que el átomo era efectivamente la particula más pequeña posible de la materia (lo cual no es cierto ya que hay partículas subatómicas)En los átomos se reconoce la existencia de partículas con carga eléctrica negativa, llamados electrones, los cuales giran en diversas "órbitas" o niveles de energía, alrededor de un núcleo central con carga eléctrica positiva. El átomo en su conjunto y sin la presencia de perturbaciones externas es eléctricamente neutro.
Dentro del átomo encontramos:
EL ELECTRÓN : Es una partícula elemental con carga eléctrica negativa igual a 1,602 x 10-19 Coulomb y masa igual a 9,1083 x 10-28 g, que se encuentra formando parte de los átomos de todos los elementos
EL NEUTRÓN: Es una partícula elemental eléctricamente neutra y masa ligeramente superior a la del protón, que se encuentra formando parte de los átomos de todos los elementos
EL PROTÓN: Es una partícula elemental con carga eléctrica positiva igual a 1,602 x 10-19 Coulomb y cuya masa es 1837 veces mayor que la del electrón. La misma se encuentra formando parte de los átomos de todos los elementos.
En un átomo de un elemento cualquiera se tiene la misma cantidad de protones y de electrones . Esta cantidad recibe el nombre de número atómico, y se designa por la letra "Z".
A la cantidad total de protones más neutrones presentes en un núcleo atómico se denomina número másico y se designa por la letra "A".
Si designamos por "X" a un elemento químico cualquiera, su número atómico y másico se representa por la siguiente simbología:
A
X
z
Por ejemplo, para el Sodio tenemos:

Así el número de neutrones resulta de la ecuacion neutrones (n) = A - Z
7/8/11
Guia para nombrar compuestos quimicos
Conocer los nombres de los compuestos en QUIMICA es muy importante. Es parte del conocimiento base para entender la materia. No sepuede avanzar en un problema de quimica si cuando se dice Oxido de Calcio o acido clorhidrico no se sabe de que se esta hablando.
Hay una serie de reglas y parámetros a seguir para nombrar correctamente los compuestos químicos.
Aquí les presento una guía resumida sobre NOMENCLATURA DE COMPUESTOS INORGANICOS. La misma se ha separado en compuestos inorgánicos principales como sales, óxidos, hidruros etc. Para los detalles especificos de como nombrar cada uno de los principales compuestos quimicos hace click en los links de abajo.
Nomenclatura Iones
Nomenclatura de Sales
Nomenclatura de Hidruros
Nomenclatura de Hidróxidos
Nomenclatura de Óxidos
Hay una serie de reglas y parámetros a seguir para nombrar correctamente los compuestos químicos.
Aquí les presento una guía resumida sobre NOMENCLATURA DE COMPUESTOS INORGANICOS. La misma se ha separado en compuestos inorgánicos principales como sales, óxidos, hidruros etc. Para los detalles especificos de como nombrar cada uno de los principales compuestos quimicos hace click en los links de abajo.
Nomenclatura Iones
Nomenclatura de Sales
Nomenclatura de Hidruros
Nomenclatura de Hidróxidos
Nomenclatura de Óxidos
Obviamente esta lista no esta completa. Para profundizar consulta los libros de quimica
6/8/11
¿De que se trata la Quimica?
La química es una rama del conocimeinto que estudia la composición, estructura y propiedades de la materia asi como los cambios que ésta experimenta durante las reacciones químicas y su relación.
La química es un area de estudio amplio y cambiante. Podemos hablar de ramas de la quimica como subespecialidades de la misma. He aqui las ´principales:
Química inorgánica: estudio de las propiedades eléctricas, magnéticas y ópticas de los compuestos formados por átomos que no sean de carbono (aunque con algunas excepciones).
Química orgánica: estudio de los compuestos que se basan en cadenas de carbono.
Química analítica: etección (identificación) y cuantificación (determinación) de una sustancia en una muestra.
Bioquímica: estudia las reacciones químicas en los seres vivos, estudia el organismo y los seres vivos.
Química física: estudia los fundamentos y bases físicas de los sistemas y procesos químicos.
QUIMICA APLICADA SEGUNDO CUATRIMESTRE 2011
Bienvenidos a este blog de apoyo para la asignatura QUIMICA APLICADA (Ingeniería).
ACLARATORIA: ESTA MATERIA NO ES COMPLICADA TAN SOLO DEBEN IR A CLASES, RESOLVER LOS PROBLEMAS DE LA GUIA Y ESTUDIAR. EL PRETENDER APROBAR SIN EL ESFUERZO DE ESTUDIO CORRESPONDIENTE ES SIMPLEMEMNTE ENGAñARSE A SI MISMO.
En Agosto comienza el Segundo Cuatrimestre del 2011
Esta asignatura posee dos actividades presenciales: teoricos y practicos.
Respecto a los practicos Uds ya se debe haber inscrito en una comision (por Sistema Guarani) y debe asistir (OBLIGATORIAMENTE) a esa comision.
Tambien hay varios horarios para consultas (hay muchas oportunidades). Las consultas son para aclarar dudas sobre la materia pero NO PARA que el PROFESOR LES RESUELVA LOS PROBLEMAS. UDs debe estudiar para que la consulta sea mas efectiva. Pueden asistir a cualquier Horario de Consulta con cualquier PROFESOR
Suscribirse a:
Comentarios (Atom)
Entrada destacada
-
Las celdas electroquímicas pueden ser de dos tipos: galvánicas o electrolíticas. Las celdas galvánicas (también llamadas voltáicas) almace...
-
Para explicar las propiedades características de los metales (su alta conductividad eléctrica y térmica, ductilidad y maleabilidad, ...) s...